مركبات تخالف قاعدة الثمانية
بعض المركبات التساهمية لا تنطبق عليها قاعدة الثمانية؛ فأحياناً يكون عدد الإلكترونات المحيطة بالذرة المركزية أقل أو أكثر من ثمانية.
الجدول التالي يبين بعض تلك المركبات:
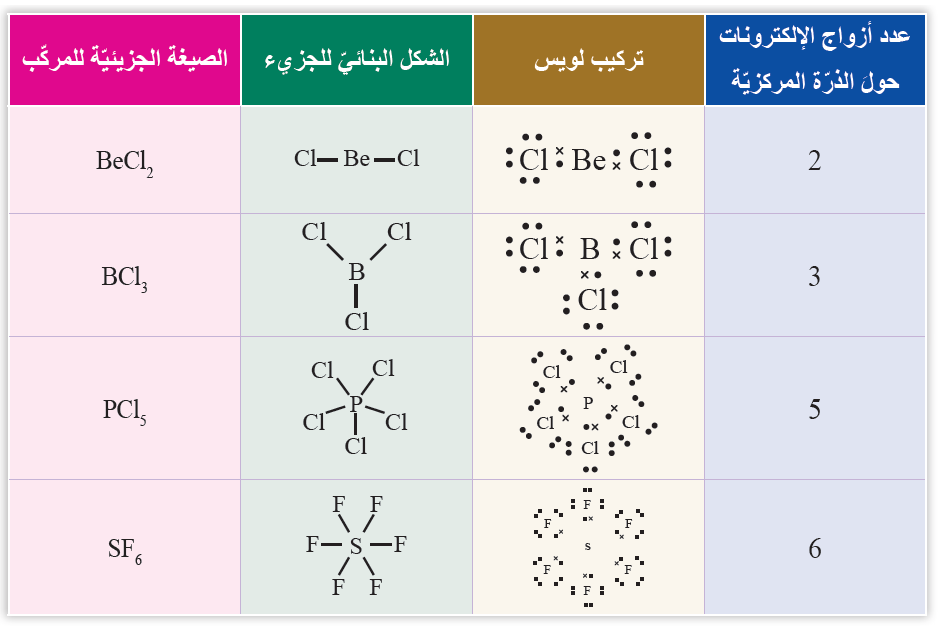
لتوضيح ذلك لنأخذ الأمثلة التالية:
مثال (1):
أكتب تركيب لويس لجزيء BeCl2 ، وأحدد عدد أزواج الإلكترونات الرابطة وغير الرابطة حول الذرة المركزية. علماً بأن العدد الذري لذرة البريليوم Be = 4 ، و Cl = 17
الحل:
أولاً: أحدد عدد إلكترونات التكافؤ لذرات الجزيء:
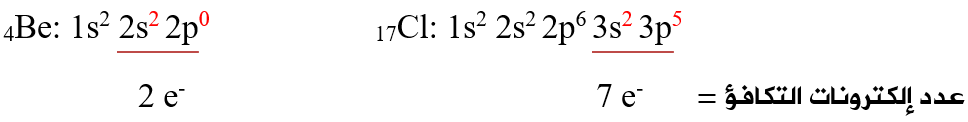
ثانياً: أحسب عدد إلكترونات التكافؤ الكلي لجميع ذرات الجزيء:
عدد إلكترونات التكافؤ الكلي = (عدد إلكترونات تكافؤ Be × عدد ذراته) + (عدد إلكترونات تكافؤ Cl × عدد ذراته)
Total (v.e) = (2 x 1) + (7 x 2) = 16e-
ثالثاً: أحسب عدد أزواج إلكترونات التكافؤ (v.e.p):
n(v.e.p) = = 8
رابعاً: أوزع ذرات Cl حول الذرة المركزية Be ، وأرسم رابطة أحادية بين ذرة البريليوم وذرات الكلور، وتمثل كل رابطة زوج رابط من الإلكترونات (b.e.p).

خامساً: أحسب عدد أزواج الإلكترونات المتبقية (l.e.p) وتساوي:
n(l.e.p) = n(v.e.p) – n(b.e.p) = 8 – 2 = 6
سادساً: أوزع الأزواج المتبقية على ذرات الكلور بحيث أحقق قاعدة الثمانية:

لاحظ أن قاعدة الثمانية انطبقت على ذرتي الكلور ولم تنطبق على ذرة البريليوم، وأن عدد أزواج الإلكترونات حول ذرة البريليوم أقل من (8).
- عدد أزواج الإلكترونات الرابطة: (2) زوج.
- عدد أزواج الإلكترونات غير الرابطة على الذرة المركزية: (0) زوج.
- عدد أزواج الإلكترونات غير الرابطة على كل ذرة كلور: (3) أزواج.
- عدد أزواج الإلكترونات غير الرابطة في الجزيء: (6) أزواج.
مثال (2):
أكتب تركيب لويس لجزيء PCl5 ، وأحدد عدد أزواج الإلكترونات الرابطة وغير الرابطة حول الذرة المركزية. علماً بأن العدد الذري لذرة الفسفور P = 15 ، والكلور Cl = 17
الحل:
أولاً: أحدد عدد إلكترونات التكافؤ لذرات الجزيء:
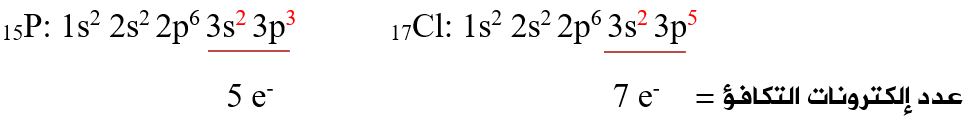
أولاً: أحسب عدد إلكترونات التكافؤ الكلي لجميع ذرات الجزيء:
عدد إلكترونات التكافؤ الكلي = (عدد إلكترونات تكافؤ P × عدد ذراته) + (عدد إلكترونات تكافؤ Cl × عدد ذراته)
Total (v.e) = (5 x 1) + (7 x 5) = 26e-
ثانياً: أحسب عدد أزواج إلكترونات التكافؤ (v.e.p):
n(v.e.p) = = 20
ثالثاً: أوزع ذرات Cl حول الذرة المركزية P ، وأرسم رابطة أحادية بين ذرة الفسفور وذرات الكلور، وتمثل كل رابطة زوج رابط من الإلكترونات (b.e.p).
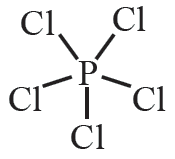
رابعاً: أحسب عدد أزواج الإلكترونات المتبقية (l.e.p) وتساوي:
n(l.e.p) = n(v.e.p) – n(b.e.p) = 20 – 5 = 15
خامساً: أوزع الأزواج المتبقية على ذرات الكلور بحيث أحقق قاعدة الثمانية:
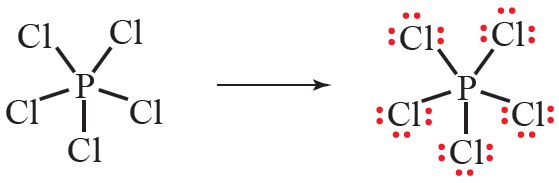
لاحظ أن قاعدة الثمانية انطبقت على ذرات الكلور ولم تنطبق على ذرة الفسفور، وأن عدد أزواج الإلكترونات حول ذرة الفسفور أكثر من (8).
- عدد أزواج الإلكترونات الرابطة: (5) أزواج.
- عدد أزواج الإلكترونات غير الرابطة على الذرة المركزية: (0) زوج.
- عدد أزواج الإلكترونات غير الرابطة على كل ذرة كلور: (3) أزواج.
- عدد أزواج الإلكترونات غير الرابطة في الجزيء: (15) زوج.
إعداد : أ. أحمد الحسين
16 / 09 / 2022
النقاشات