التهجين من نوع sp
تجري الذرات المركزية تهجيناً من نوع sp إذا اختلط فلك من نوع s من الذرة المركزية، مع فلك من نوع p من الذرة نفسها، فيتكون فلكين مهجنين من نوع sp ويتجه الفلكين المهجنين في الفراغ بحيث يكون التنافر بين إلكتروناتها أقل ما يمكن فتأخذ شكلاً خطياً، والزاوية فيما بينهما 180o
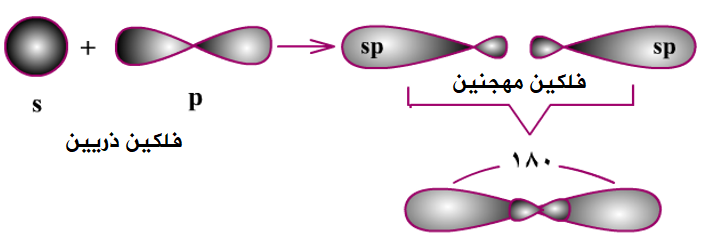
مثال: جزيء BeF2
انظر إلى التوزيع الإلكتروني لذرة البريليوم المركزية:
4Be:[He] 2s2 2p0
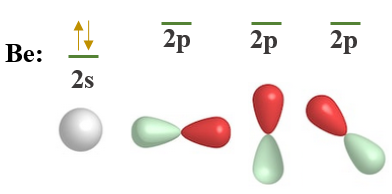
ومن التوزيع الإلكتروني تلاحظ أن ذرة البريليوم لا تحتوي على إلكترونات منفردة، لذا فليس لها القدرة على الارتباط مع ذرتي فلور، حسب نظرية رابطة التكافؤ، والتي تحدد من خلالها عدد الروابط من خلال عدد الإلكترونات المنفردة.
ولكي ترتبط ذرة البريليوم بذرتي فلور، يجب أن يكون لديها إلكترونين منفردين، وعليه تقوم ذرة البريليوم بعمل ترقية للإلكترون من المستوى الفرعي 2s إلى أحد أفلاك المستوى الفرعي 2p الفارغة.
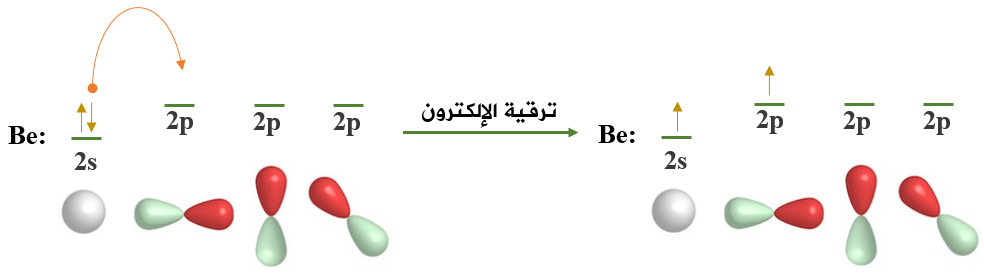
ولكي تكوّن ذرة البريليوم رابطتين متكافئتين مع ذرتي فلور تقوم بمساواة طاقة الفلكين اللذين يحتويان على إلكترونين منفردين، وتخلطهما معاً لتكوين فلكين مهجنين يسمى كل منهما sp ، مع بقاء فلكين ذريين فارغين من نوع 2p في ذرة البريليوم.
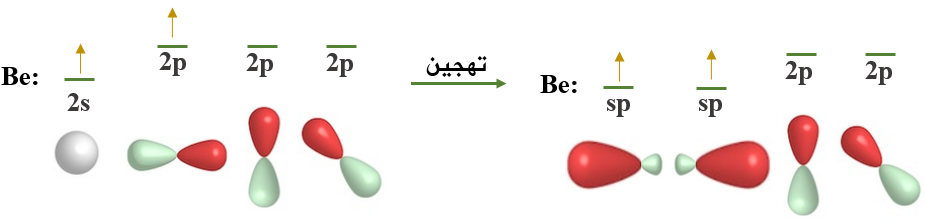
يتجه الفلكين المهجنين في الفراغ باتجاهين متعاكسين بحيث يكون التنافر بين إلكتروناتهما أقل ما يمكن ويأخذ الفلكين شكلاً خطياً، والزاوية 180o
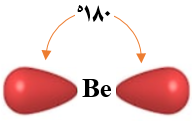
ثم تقدّم كل ذرة فلور فلكاً ذرياً من نوع إلى كل فلك مهجن 2p .
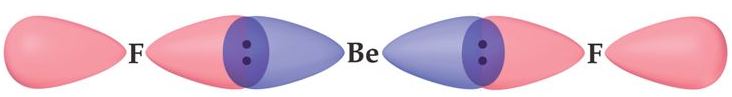
- نوع التهجين الذي تجريه ذرة البريليوم: sp
- عدد الأفلاك المهجنه في ذرة البريليوم: 2
- الشكل الهندسي (البنائي) لجزيء BeF2 : خطي مستقيم.
- قيمة الزاوية بين الأفلاك المهجنة: 180o
- نوع الأفلاك الداخلة في تكوين الرابطة sp-p : Be-F .
- مبرر التهجين: تفسير عدد الروابط.
إعداد : أ. أحمد الحسين
03 / 11 / 2022
النقاشات