 |

الإسترات: مركبات عضوية غير مشبعة، وتحمل الصيغة العامة:

(يمكن أن تكون R' ذرة هيدروجين).
وتشتق الإسترات من تفاعل الكحول مع الحمض الكربوكسيلي.
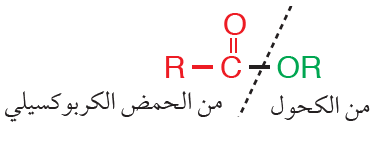
تحمل الإسترات الصيغة الجزيئية العامة:
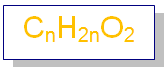
لاحظ أن الصيغة الجزيئية للإسترات مشابهة للصيغة الجزيئية للحموض الكربوكسيلية، فهما بذلك متصاوغات وظيفية.
تتميز الإسترات برائحة عطرة تشبه رائحة بعض أنواع الفواكه، إلا أن هذا لا يعني بالضرورة وجود هذه الإسترات في الفواكه.
قواعد التسمية النظامية للإسترات:
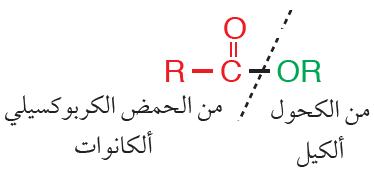
- أسمي الجزء المشتق من الحمض الكربوكسيلي على وزن الكانوات.
- أسمي الجزء المشتق من الكحول على وزن ألكيل.
مثال (1):
أسمي المركب الآتي:
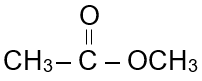
الجزء الأيسر من الإستر مشتق من حمض الإيثانويك، فأسميه إيثانوات، والجزء الأيمن من الإستر مشتق من الميثانول، فأسميه الميثيل:
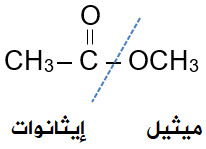
فيصبح الاسم:
إيثانوات الميثيل
مثال (2):
أسمي المركب الآتي:
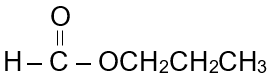
الجزء الأيسر من الإستر مشتق من حمض الميثانويك، فأسميه ميثانوات، والجزء الأيمن من الإستر مشتق من البروبانول، فأسميه البروبيل:
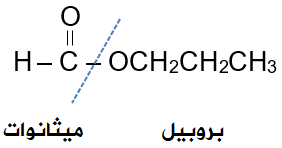
فيصبح الاسم:
ميثانوات البروبيل
مثال (3):
أسمي المركب الآتي:
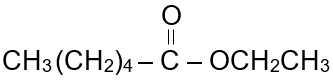
الجزء الأيسر من الإستر مشتق من حمض الهكسانويك، فأسميه هكسانوات، والجزء الأيمن من الإستر مشتق من الإيثانول، فأسميه الإيثيل:
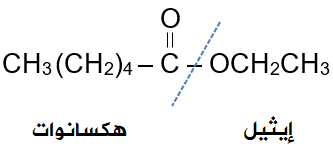
فيصبح الاسم:
هكسانوات الإيثيل
سؤال (1):
أسمّي المركبين العضويين التاليين حسب التسمية النظامية:
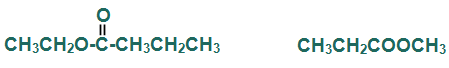
سؤال (2):
اكتب الصيغ البنائية للمركبين العضويين التاليين:
أ- بروبانوات البروبيل.
ب- ميثانوات البيوتيل.
الخواص الفيزيائية للإسترات
الإسترات مركبات قطبية، وعليه فجزيئاتها تترابط بقوى ثنائية القطب التي تعتمد على الكتلة المولية.