مفهوم أرهينيوس
Arrhenius Concept of Acid and Base
الحمض: المادة الكيميائية التي تتفكك في الماء فتزيد من تركيز أيونات الهيدروجين (H+) فيه.
شروط الحمض وفق مفهوم أرهينيوس:
- يجب أن يذاب في الماء.
- يجب أن يحتوي على هيدروجين.
مثال على حمض أرهينيوس:
حمض الهيدروكلوريك حمض قوي يتفكك بالكامل عند إذابته في الماء منتجاً أيونات (H+)، وفق المعادلة:

سؤال:
تنتمي المواد الآتية إلى الحموض حسب تعريف أرهينيوس (HClO4 , HNO3 , HBr).
- سمّ هذه المواد.
- اكتب المعادلة الكيميائية التي تمثل تأين كلّ منها في الماء.
الحل:
1- أسماء الحموض:
حمض الهيدروبروميك: HBr
حمض النتريك: HNO3
حمض البيركلوريك: HClO4
2-
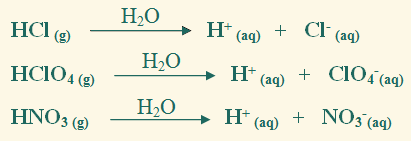
القاعدة: المادة الكيميائية التي تتفكك في الماء فتزيد من تركيز أيونات الهيدروكسيد (OH-) فيه.
شروط القاعدة وفق مفهوم أرهينيوس:
- يجب أن تذاب في الماء.
- يجب أن تحتوي على هيدروكسيد.
مثال على قاعدة أرهينيوس:
هيدروكسيد الصوديوم قاعدة قوية تتفكك بالكامل عند إذابتها في الماء منتجةً أيونات (OH-)، وفق المعادلة:

محددات تعريف أرهينيوس:
- افترض أرهينيوس أن جميع القواعد يجب أن تحتوي على مجموعة الهيدروكسيد، وفي الحقيقة فإن هنالك العديد من القواعد التي لا تحتوي على هيدروكسيد مثل الأمونيا (NH3).
- عجز التعريف عن تفسير الصفات الحمضية أو القاعدية لمحالي بعض الأملاح، مثل NaF و NH4Cl .
- لم يحدد أرهينيوس الدور الرئيس للمذيب (الماء) في عملية تأيين الحمض أو القاعدة.
- اقتصر التعريف على المحاليل المائية، وعليه لا يمكن اعتبار غاز كلوريد الهيدروجين HCl حمضاً ما لم يذب في الماء.
أيون الهيدرونيوم
وفقاً لتعريف أرهينيوس، يُنتج الحمض أيون الهيدروجين (H+) عند إذابته في الماء، وحيث أن أيون الهيدروجين يتكون من بروتون واحد صغير الحجم، فإن كثافة الشحنة الموجبة عليه تكون عالية جداً، ولذا لا يتواجد حراً في الماء، بل يرتبط بعدد من جزيئات الماء أقلها واحد، مكوناً أيون يُعرف بأيون الهيدرونيوم.

إعداد : شبكة منهاجي التعليمية
21 / 01 / 2023
النقاشات