تفاعل فلزات المجموعة الأولى مع الماء
تعد عناصر المجموعة الأولى من أنشط العناصر، ويجب التعامل معها بحذر شديد.

تتفاعل فلزات المجموعة الأولى كالصوديوم والليثيوم والبوتاسيوم مع الماء البارد، وتعطي النواتج نفسها، إلا أنها تتفاوت في شدة تفاعلها مع الماء.
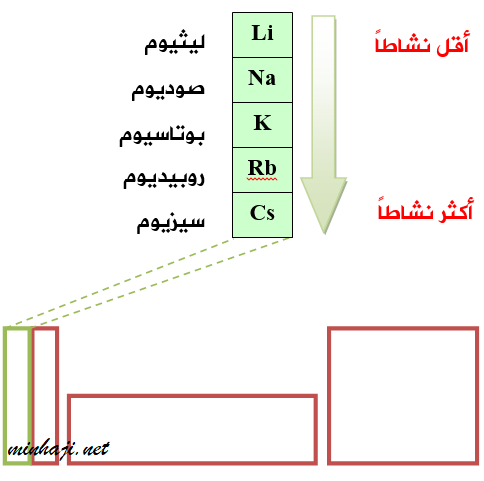
تتفاعل فلزات المجموعة الأولى بقوة مع الماء البارد، وتزداد قوة التفاعل عند استخدام الماء الساخن، ويصبح التفاعل عنيفاً جداً مع البخار.
تفاعل الليثيوم مع الماء
يتفاعل الليثيوم مع الماء البارد، وينتج محلول هيدروكسيد الليثيوم (محلول قاعدي)، ويتصاعد غاز الهيدروجين.
ليثيوم (صلب) + ماء (سائل) ← هيدروكسيد الليثيوم (محلول) + هيدروجين (غاز) + طاقة حرارية
ويمكن تمثيل التفاعل بالمعادلة الرمزية التالية:
2Li (s) + 2H2O (l) → 2LiOH (aq) + H2 (g)
تفاعل البوتاسيوم مع الماء
وبالطريقة نفسها يمكن كتابة تفاعل البوتاسيوم مع الماء.
بوتاسيوم (صلب) + ماء (سائل) ← هيدروكسيد البوتاسيوم (محلول) + هيدروجين (غاز) + طاقة حرارية
ويمكن تمثيل التفاعل بالمعادلة الرمزية التالية:
2K (s) + 2H2O (l) → 2KOH (aq) + H2 (g)
إعداد : شبكة منهاجي التعليمية
05 / 12 / 2018
النقاشات