رابعاً: درجة الحموضة pH
تنتج الحموض عند تأينها في الماء أيونات H+ .
كلما زاد تركيز أيونات H+ في محلول الحمض زادت حامضيته.
تنتج القواعد عند تأينها في الماء أيونات OH- .
كلما زاد تركيز أيونات OH- في محلول القاعدة زادت قاعديته.
تم الاتفاق على وضع تدريج (0 – 14) يعبر عن درجة حموضة المحلول.
درجة الحموضة: هو مقياس لتحديد تركيز أيونات الهيدروجين H+ في المحلول.
يُرمز لدرجة الحموضة بالرمز (pH)، وتُعرف أيضاً بالرقم الهيدروجيني.
درجة الحموضة مقياس مدرّج من 0 إلى 14 ويُعبّر عن تركيز أيونات H+ وأيونات OH- في المحلول.
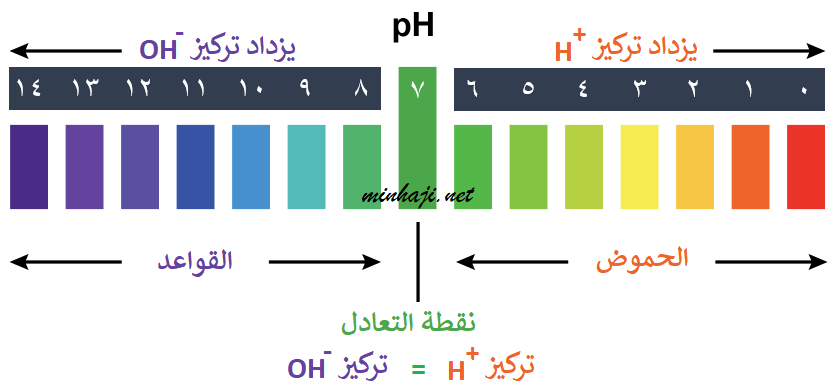
فالمحاليل الحمضية تمتلك قيمة pH أقل من (7)، وكلما قلت قيمة pH للحمض زادت حامضيته.
والمحاليل القاعدية تمتلك قيمة pH أكبر من (7)، وكلما زادت قيمة pH للقاعدة زادت قاعديته.
أما الماء المقطر فتبلغ قيمة pH له (7)، أي أنه يُعتبر متعادلاً وفق هذا المقياس لأن تركيز أيونات H+ مساوٍ لتركيز أيونات OH- .
الشكل التالي يمثل قيم درجة الحموضة لبعض المواد الشائعة:
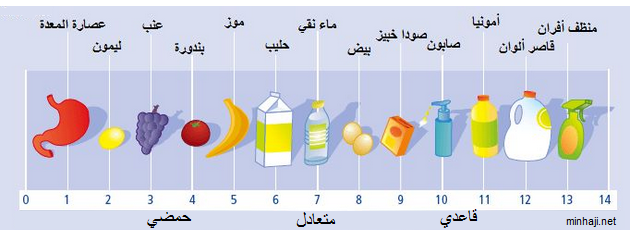
قياس درجة الحموضة
أولاً: الكاشف العام
الكاشف العام: مزيج من الكواشف، يمتاز بأن لونه يتغير بتغير قيم pH للمحلول.

انظر ألى ألوان أوراق الكاشف العام عند استخدام عن درجة الحموضة لبعض المواد:

سؤال:
ما الفرق بين استخدام الكاشف العام وكاشف تباع الشمس أو الفينولفثالين.
ثانياً: جهاز قياس الرقم الهيدروجيني
وهو أكثر دقة من الكاشف العام.

إعداد : شبكة منهاجي التعليمية
19 / 07 / 2022
النقاشات