سادساً: تحضير الحموض والقواعد صناعياً
أولاً: هيدروكسيد الصوديوم NaOH
 خصائص هيدروكسيد الصوديوم:
خصائص هيدروكسيد الصوديوم:
- مادة بيضاء صلبة.
- سريعة الذوبان في الماء.
- لها ملمس صابوني.
- لها تأثير كاوٍ على الجلد.
استخدامات هيدروكسيد الصوديوم:
- صناعة الورق.
- صناعة الزجاج.
- صناعة الحرير الطبيعي والنسيج.
- صناعة الصابون من الزيوت النباتية.
تحضير هيدروكسيد الصوديوم:
يحضر بطريقة التحليل الكهربائي لمحلول كلوريد الصوديوم في خلية داون.
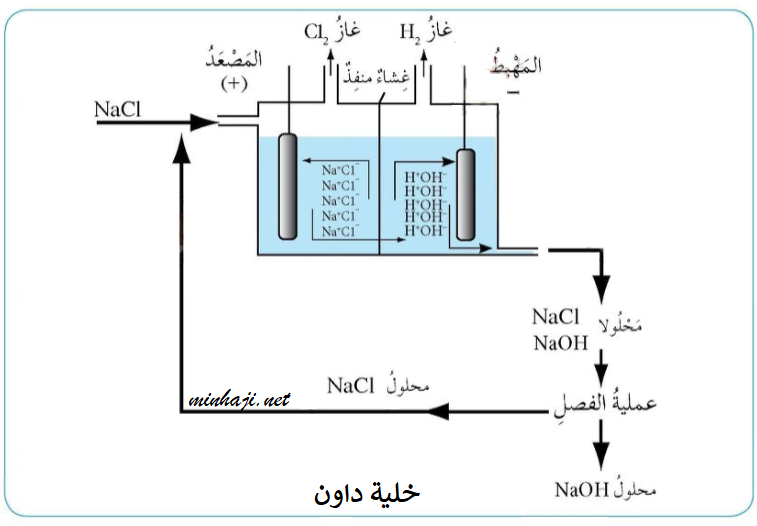
يتصاعد غاز H2 على المهبط، وغاز Cl2 على المصعد.
يحضر في خلية داون وفق المعادلة:

ثانياً: الأمونيا (النشادر) NH3
خصائص الأمونيا:
- غاز عديم اللون.
- أخف من الهواء.
- له رائحة نفاذة تُسبب تهيجاً شديداً لأعضاء التنفس والعيون.
- تسهل إسالته بالتبريد أو الضغط.
- سريع الذوبان في الماء.
استخدامات الأمونيا:
- وسيلة تبريد في المصانع الكبيرة.
- يستخدم في الصناعات التعدينية.
- يستخدم في عجينة الورق.
- يستخدم في اللدائن.
- يستخدم في النايلون.
- يستخدم في الألياف الصناعية.
- يستخدم في دباغة الجلود.
- يستخدم في صناعة المنظفات المنزلية.
- يستخدم في صناعة العقاقير.
- يستخدم في صناعة مواد كيميائية عديدة، مثل: حمض النيتريك، والأعلاف، والأسمدة النيتروجينية كسماد اليوريا.
تحضير الأمونيا:
تحضر بطريقة هابر من التفاعل المباشر بين النيتروجين والهيدروجين.
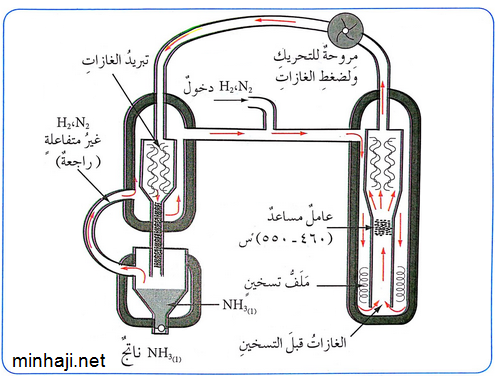
يحضر بطريقة هابر وفق المعادلة:

ثالثاً: حمض الكبريتيك H2SO4
خصائص حمض الكبريتيك:
- الحمض المركز منه سائل كثيف القوام كثافته 1,84 غ/مل.
- يعتبر من أقوى الحموض.
- حارق للجلد كغيره من الحموض، ومهيج للأنسجة المبطنة للأنف والقصبات الهوائية والرئتين.
- يذوب بشدة في الماء، وعند ذوبان حمض الكبريتيك المركز في الماء تنتج حرارة كافة تؤدي إلى غليان المحلول، لذلك عند تخفيف محلوله يجب إضافة الماء ببطء؛ كي لا يسبب إضافة الماء إلى غليان المحلول وتطايره.
استخدامات حمض الكبريتيك:
- صناعة بطاريات السيارات.
- صناعة الأسمدة الفوسفاتية.
- صناعة الأصباغ المستخدمة في دباغة الجلود.
- صناعة الورق.
- صناعة البلاستيك والمطاط.
تحضير حمض الكبريتيك:
قديماً:
حمض الكبريتيك معروف قديماً، فقد أطلق عليه جابر بن حيّان اسم "زيت الزاج"، وكان يحضر من الزاج الأخضر (كبريتات الحديد المائية).
حديثاً:
يحضر حمض الكبريتيك بطريقة التلامس (التماس)، وهي الطريقة الأوسع استخداماً والأقل كلفة؛ لأن حمض الكبريتيك فيها يكون نقياً، وبتركيز 98%.
خطوات تحضير حمض الكبريتيك بطريقة التلامس:
- يُصهر الكبريت ويرشح؛ لفصل الأجزاء غير المنصهرة عنه.
- يضخ الكبريت المنصهر إلى مفاعل حراري، حيث يتأكسد الكبريت للحصول على ثاني أكسيد الكبريت SO2 .
- يمرر الغاز إلى مرشح الغاز لتنقيته من الشوائب.
- ينقل الغاز إلى برج التحويل المحتوي على عامل مساعد مثل أكسيد الفاناديوم (V2O5)، فيتأكسد إلى ثالث أكسيد الكبريت (SO3)، ثم يتحد الغاز مع الماء لإنتاج حمض الكبريتيك وفق المعادلتين:
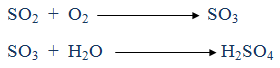
- يمرر الحمض الناتج إلى برج التبريد، ويتم التحكم بتركيز الحمض عن طريق التبريد والتبخير.
رابعاً: حمض الفسفوريك H3PO4
استخدامات حمض الفسفوريك:
- يعد حمض الفسفوريك مصدراً أساسياً للفسفور اللازم لنمو النبات.
- يستخدم حمض الفسفوريك في إنتاج الأسمدة الفوسفاتية حسب المعادلة:
تحضير حمض الفسفوريك:
يحضر حمض الفسفوريك من خام الفوسفات بالخطوات التالية:
- ينقل الفوسفات من المناجم إلى مصنع حمض الفسفوريك في العقبة.
- يطحن الفوسفات حتى يصبح حبيبات صغيرة.
- ينتج حمض الفسفوريك من تفاعل فوسفات الكالسيوم في الخام مع حمض الكبريتيك حسب المعادلة:

- ينقل حمض الفسفوريك إلى خزانٍ خاص، ويباع جزء منه للسوق المحلي ويصدر الباقي للخارج.
إعداد : أ. أحمد الحسين
21 / 04 / 2020
النقاشات