
مركبات عضوية تحمل الصيغة العامة RX حيث X هالوجين ( F , Cl , Br , I )، وتعد ذرة الهالوجين المجموعة الوظيفية في هاليدات الألكيل.
قواعد التسمية النظامية لهاليدات الألكيل:
- أختار أطول سلسلة كربونية متتابعة مرتبطة بذرة الهالوجين.
- أرقم السلسلة من الطرف الأقرب لذرة الهالوجين.
- أسمي التفرع (على وزن ألكيل) إن وجد مسبوقاً برقم ذرة الكربون المرتبطة به، أو أسمي الهالوجين على وزن هالو (فلورو، كلورو، برومو، أيودو)، ويعتمد ترتيب التفرعات والهالوجينات في التسمية على الترتيب الهجائي.
- أسمّي السلسلة الطويلة كما تسمى الألكانات.
مثال (1):
أسمي المركب الآتي وفق نظام الأيوباك.
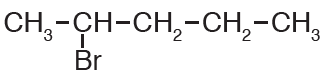
أولاً: أختار أطول سلسلة كربونية متتابعة.
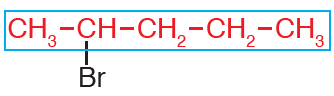
ثانياً: أرقم السلسلة من الطرف الأقرب للهالوجين (Br).
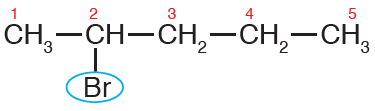
ثالثاً: أضع رقم ذرة الكربون المرتبطة بالهالوجين، ثم أسمي الهالوجين على وزن هالو (برومو)، ثم أسمي أطول سلسلة كما تسمى الألكانات (بنتان)، فيصبح اسم المركب:
2- برومو بنتان
مثال (2):
أسمي المركب الآتي وفق نظام الأيوباك.
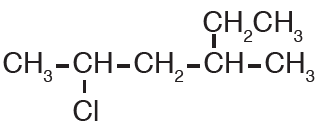
أولاً: أختار أطول سلسلة كربونية متتابعة.
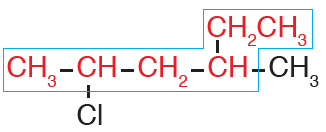
ثانياً: أرقم السلسلة من الطرف الأقرب للهالوجين (Cl).
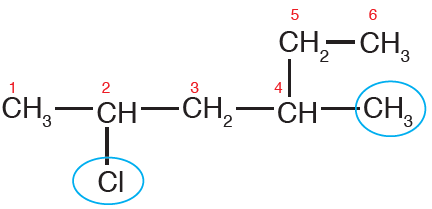
ثالثاً: أسمي الهالوجين أولاً لأن (كلورو) يسبق (ميثيل) هجائياً، مسبوقاً كل منهما برقم ذرة الكربون المرتبط بها.
2-كلورو -4- ميثيل هكسان
مثال (3):
أسمي المركب الآتي وفق نظام الأيوباك.
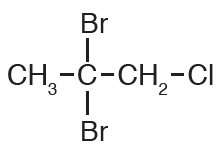
أولاً: أختار أطول سلسلة كربونية متتابعة.
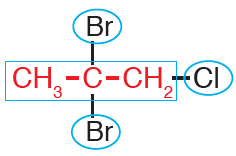
ثانياً: أرقم السلسلة من الطرف الأقرب للهالوجين (Cl).
ثالثاً: أسمي ذرتي البروم أولاً على وزن هالو (برومو) وأسبق التسمية بكلمة ثنائي، ثم أسمي الكلور على وزن هالو (كلورو)، ثم أسمي أطول سلسلة كما تسمى الألكانات (بروبان)، فيصبح اسم المركب:
2، 2- ثنائي برومو-1-كلورو بروبان
أمثلة إضافية:
لاحظ طريقة تسمية هاليدات الألكيل الآتية:
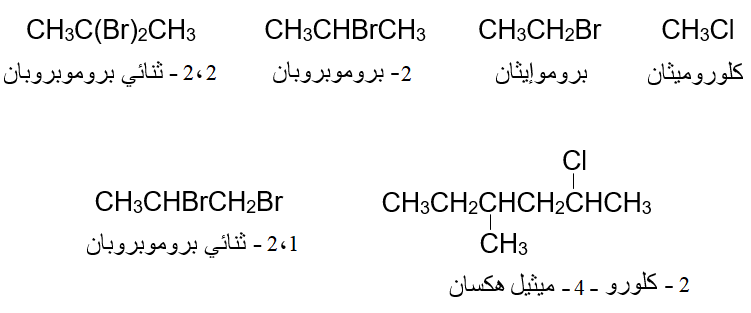
سؤال 1 :
أسمّي المركبات العضوية التالية وفق نظام الأيوباك:
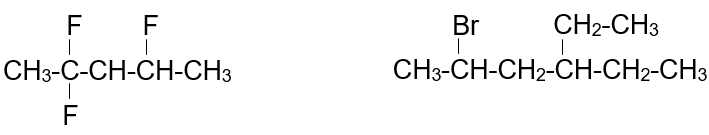
سؤال 2 :
أكتب الصيغة البنائية للمركب العضوي التالي:
1- كلورو – 5 – إيثيل -3- ميثيل هبتان.
الخصائص الفيزيائية لهاليدات الألكيل
هاليدات الألكيل مركبات قطبية نظراً لاختلاف لارتفاع السالبية الكهربائية لمعظم الهالوجينات ، لذا تترابط جزيئاتها بقوى ثنائية القطب.
درجات الغليان
درجات غليان هاليدات الألكيل أعلى من الهيدروكربونات المقاربة لها في الكتلة المولية، كما أن درجات غليانها تزداد بزيادة الكتلة المولية للهالوجين إذا ارتبطوا بعدد مماثل من ذرات الكربون.
لاحظ اختلاف درجات غليان الإيثان مقارنة بهاليدات الألكيل المقابلة لها:
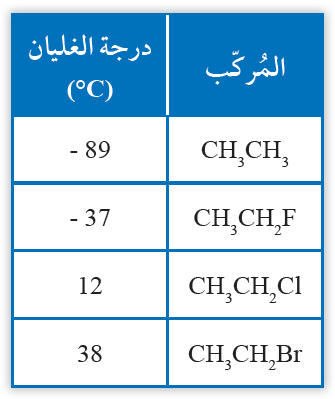
سؤال:
رتب هاليدات الألكيل الآتية وفقاً لتزايد درجة غليانها:
CH3CH2CH2Br , CH3CH2CH2Cl , CH3CH2CH2I
الحالة الفيزيائية
تتواجد معظم هاليدات الألكيل في الحالة السائلة أو الصلبة في درجة الحرارة العادية.
الذائبية في الماء
رغم كون هاليدات الألكيل قطبية إلا أنها لا تذوب في الماء؛ لأن قوى ثنائية القطب التي تنشأ بين هاليدات الألكيل والماء ضعيفة لا تستطيع التغلب على الروابط الهيدروجينية بين جزيئيات الماء.
الأهمية الصناعية لهاليدات الألكيل
تستخدم هاليدات الألكيل مباشرة في الصناعة، أو كمادة أولية لتحضير مركبات أخرى.
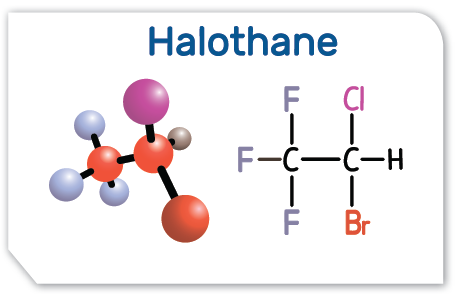
- استخدم الكلوروفورم CHCl3 قديماً كمادة مخدرة في العمليات الجراحية، وبسبب آثاره الجانبية حل محله هاليد ألكيل آخر سمي الهالوثان.
- تستخدم هاليدات الألكيل كمذيبات عضوية، مثل ثلاثي كلورو إيثين C2HCl3 الذي يستخدم في الصناعات الإلكترونية.
- استخدم ثلاثي كلورو فلورو ميثان CCl3F كمادة نفخ في صناعة البلاستيك الرغوي (الفوم).
- يستخدم كلورو إيثين في صناعة أكثر أنواع البلاستيك استخداماً، حيث يستخدم في تمديدات شبكات المياه والصرف الصحري.
- تستخدم بعض المركبات الهيدروفوروكربونية كغازات مبردة في الثلاجات وأجهزة التبريد.
إعداد : أ. أحمد الحسين
20 / 03 / 2024
النقاشات