ثالثاً: تفاعلات الإزاحة
تفاعلات الإزاحة: هي التفاعلات التي يحلّ فيها عنصر نشيط كيميائيًا محل عنصر أقلّ نشاطًا كيميائيًا منه.
وتُعرف أيضاً بتفاعلات التبادل الأحادي.
الشكل العام لمعادلة تفاعلات الإزاحة:
A + BC → AC + B
ولإتمام تفاعلات الإزاحة يجب الاضطلاع على سلسلة النشاط الكيميائي:
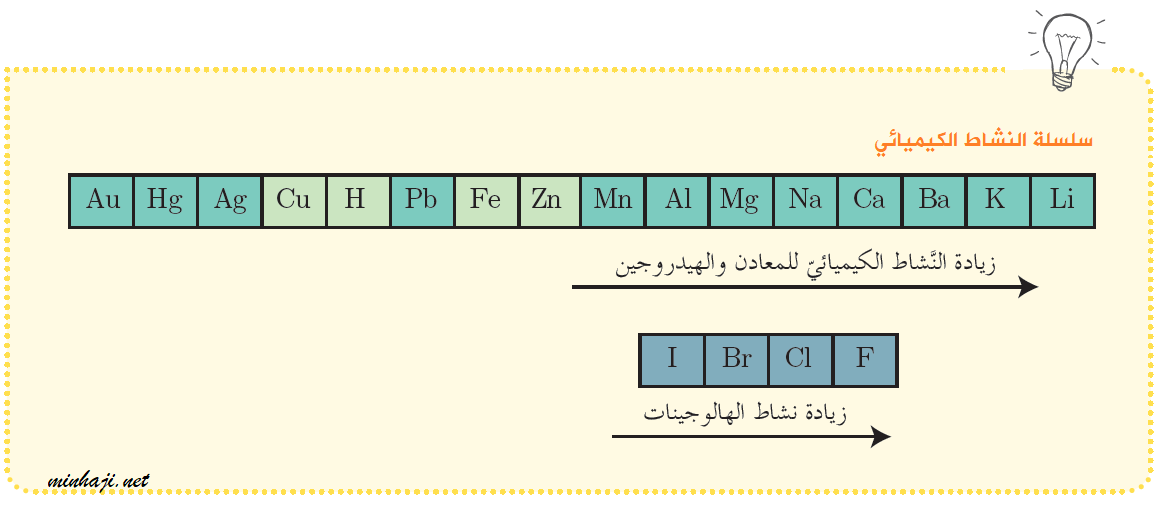
ومن السلسلة يتضح:
أن الكالسيوم يستطيع أن يزيح الصوديوم من مركباته، بينما لا يستطيع الصوديوم أن يزيح الكالسيوم من مركباته.
وأنّ الكلور يستطيع أن يزيح البروم من مركباته، بينما لا يستطيع البروم أن يزيح الكلور من مركباته.
مثال (1):
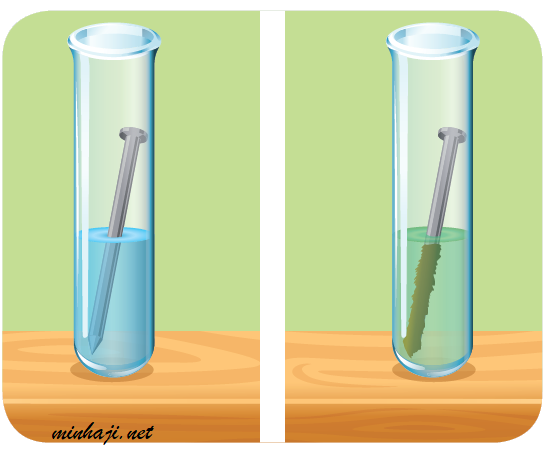
عند غمس مسمار حديد في محلول كبريتات النحاس ذو اللون الأزرق، يتشكل لون أخضر، وتترسب طبقة حمراء على مسمار الحديد.
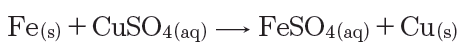
التفسير:
استطاع الحديد أن يُزيح أيونات النحاس Cu2+ ذات اللون الأزرق ليتشكل أيونات الحديد Fe2+ ذات اللون الأخضر؛ لأن الحديد أكثر نشاطاً من النحاس، وتترسب طبقة من النحاس الأحمر على مسمار الحديد.
مثال (2):
عند غمس قطعة من الزنك في محلول حمض كلور الماء تنطلق فقاعات غازية مع تآكل الزنك.

التفسير:
الزنك أكثر نشاطاً من الهدروجين، فيزيحه ويحل محله، وينطلق غاز الهدروجين، ويحدث التفاعل وفق المعادلة الآتية:
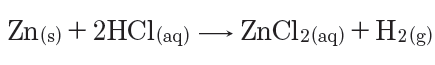

الإجابة:
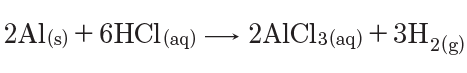
إعداد : شبكة منهاجي التعليمية
04 / 06 / 2019
النقاشات