أسئلة وزارية (التأكسد والاختزال)
الدورات (2022-2020)
خطة 2020 الطلبة النظاميون
اختر الإجابة الصحيحة في كل فقرة مما يأتي، ثم ظلل بشكل غامق الدائرة التي تشير إلى رمز الإجابة في نموذج الإجابة (ورقة القارىء الضوئي) فهو النموذج المعتمد (فقط) لاحتساب علامتك، علماً بأن عدد الفقرات (12):
1- عدد تأكسد ذرة الكلور Cl في المركب HClO3 يساوي:
أ- +1
ب- -1
ج- +5
د- -5
2- أعلى قيمة لعدد تأكسد ذرة المنغنيز Mn يكون في:
أ- Mn
ب- MnO2
ج- Mn2+
د- MnO4-
3- في التفاعل الآتي HSO3- + IO3- → SO42- + I2 فإن العامل المختزل هو:
أ- I2
ب- SO42-
ج- IO3-
د- HSO3-
4- أحد أنصاف التفاعلات الآتية يحتاج إلى عامل مؤكسد، هو:
أ- SO42- → SO2
ب- Cr2O72- → Cr3+
ج- I2O5 → I2
د- Al → AlO2-
5- عدد مولات أيونات H+ اللازمة لموازنة نصف التفاعل N2H4 → NO يساوي:
أ- 2
ب- 4
ج- 6
د- 8
- ادرس المعلومات الواردة في الجدول، وأجب عن الفقرات (6، 7، 8، 9، 10)

6- العبارة الصحيحة فيما يتعلق بخلية جلفانية قطباها Co و Ni ، هي:
أ- تقل كتلة القطب Ni
ب- شحنة قطب Co سالبة
ج- تزداد كتلة قطب Co
د- يزداد تركيز أيونات Ni2+
7- لا يمكن حفظ محلول ZnSO4 في وعاء مصنوع من:
أ- Al
ب- Cu
ج- Ni
د- Ag
8- يمكن تكوين خلية جلفانية لها أعلى فرق جهد باستخدام أقطاب من:
أ- Zn/Cu
ب- Zn/Ag
ج- Ag/Al
د- Ag/Cu
9- أقوى عامل مؤكسد، هو:
أ- Ag+
ب- Al3+
ج- Ni2+
د- Cu2+
10- في الخلية الجلفانية قطباها (Ag/Cu) تكون قيمة جهد الخلية المعياريoE (فولت) تساوي:
أ- +0.46
ب- -0.46
ج- +1.14
د- -1.14
11- العبارة الصحيحة فيما يتعلق بالخلية الجلفانية:
أ- قطب المهبط سالب.
ب- التفاعل تلقائي.
ج- قطب المصعد موجب.
د- جهد الخلية سالب.
12- الفلزات الافتراضية (C,B,A) مرتبة حسب قوتها كعوامل مختزلة (C<B<A) فالعبارة الصحيحة هي:
أ- جهد اختزال B2+ أكبر من جهد اختزال C2+
ب- ميل أيونات C2+ للاختزال أكبر من ميل أيونات A2+
ج- يمكن حفظ أملاح C في وعاء من B
د- يمكن تحريك محلول الملح B بملعقة A
الدورة التكميلية 2020 الطلبة النظاميون
اختر الإجابة الصحيحة في كل فقرة مما يأتي، ثم ظلل بشكل غامق الدائرة التي تشير إلى رمز الإجابة في نموذج الإجابة (ورقة القارىء الضوئي) فهو النموذج المعتمد (فقط) لاحتساب علامتك، علماً بأن عدد الفقرات (15):
1- عدد تأكسد ذرة البورون B في المركب BF3 ، يساوي:
أ- +3
ب- +1
ج- -3
د- -1
2- أعلى عدد تأكسد لذرة الكبريت S يكون في:
أ- S2-
ب- S8
ج- SO42-
د- HSO3-
3- العامل المختزل في التفاعل ClO3- + N2H4 → Cl- + NO ، هو:
أ- NO
ب- N2H4
ج- Cl-
د- ClO3-
4- عدد تأكسد ذرة الأكسجين يكون (-1) في المركب:
أ- Na2O
ب- CaO
ج- OF2
د- BaO2
- بناءً على المعلومات في الجدول الآتي، أجب عن الفقرتين (5، 6):
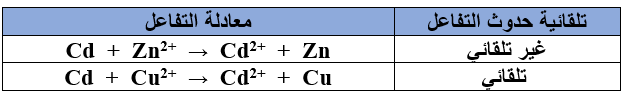
5- فإن الترتيب الصحيح لأيونات الفلزات وفقاً لقوتها كعوامل مؤكسدة، هو:
أ- Cd2+ > Cu2+ > Zn2+
ب- Zn2+ > Cu2+ > Cd2+
ج- Cd2+ > Zn2+ > Cu2+
د- Cu2+ > Cd2+ > Zn2+
6- العبارة الصحيحة من العبارات الآتية، هي:
أ- يمكن تحريك محلول كبريتات النحاس CuSO4 بملعقة من فلز الكادميوم Cd
ب- في خلية قطباها (Cd/Zn) يتجه مؤشر الغلفانوميتر نحو قطب الكادميوم Cd
ج- في خلية قطباها (Zn/Cu) يزداد تركيز أيونات النحاس Cu2+
د- يمكن حفظ محلول كبريتات الكادميوم CdSO4 في وعاء من فلز الخارصين Zn
7- نصف التفاعل الذي يحتاج إلى عامل مؤكسد:
أ- BrO3- → Br-
ب- PbO2 → Pb2+
ج- Fe2O3 → Fe
د- Cl2O → ClO3-
8- عدد مولات H+ اللازم لموازنة نصف التفاعل H2SO3 → SO42- في وسط حمضي يساوي:
أ- 1
ب- 2
ج- 4
د- 5
9- عدد مولات OH- اللازم إضافتها إلى طرفي المعادلة الآتية لموازنتها في الوسط القاعدي يساوي:
Cr2O3 + 3NO3- + 2H2O → 2CrO42- + 3NO2- + 4H+
أ- 2
ب- 4
ج- 6
د- 8
- ادرس المعلومات الواردة في الجدول المجاور، وأجب عن الفقرات (10، 11، 12، 13)، علماً بأن قيمة جهد الاختزال المعياري للهيدروجين = صفر.
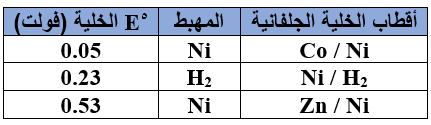
10- في الخلية الجلفانية التي قطباها (Ni/Co)، قيمة جهد الاختزال المعياري oE (فولت) لأيونات Co3+ تساوي:
أ- -0.28
ب- -0.18
ج- +0.28
د- +0.18
11- قيمة جهد الخلية المعياري oE (فولت) لخلية جلفانية قطباها (Zn/H2) تساوي:
أ- -0.23
ب- -0.76
ج- +0.23
د- +0.76
12- العامل المؤكسد الأقوى، هو:
أ- Ni2+
ب- Co2+
ج- H+
د- Zn2+
13- العبارة الصحيحة في ما يتعلق بالخلية الجلفانية التي قطباها (Ni/Zn)، هي:
أ- تقل كتلة Ni
ب- يزداد تركيز أيونات Zn2+
ج- شحنة القطب Ni سالبة
د- شحنة القطب Zn موجبة
14- خلية جلفانية قطباها (Cd/Pb)، واتجاه مؤشر الفولتميتر فيها باتجاه قطب الرصاص Pb فإن التفاعل الذي يحدث على المصعد، هو:
أ- Pb → Pb2+ + 2e-
ب- Cd → Cd2+ + 2e-
ج- Pb2+ + 2e- → Pb
د- Cd2+ + 2e- → Cd
15- إذا علمت أنه يمكن تحريك محلول كبريتات الفلز Z بملعقة من الفلز Y ولا يمكن تحريك محلول كبريتات الفلز X بالملعقة نفسها، فإن الترتيب الصحيح للعناصر X,Y,Z وفق قوتها كعوامل مختزلة هو:
أ- Y<X<Z
ب- Z<Y<X
ج- Z<X<Y
د- X<Y<Z
دورة 2021
اختر الإجابة الصحيحة في كل فقرة مما يأتي، ثم ظلل بشكل غامق الدائرة التي تشير إلى رمز الإجابة في نموذج الإجابة (ورقة القارىء الضوئي) فهو النموذج المعتمد (فقط) لاحتساب علامتك، علماً بأن عدد الفقرات (10):
1- يسلك الأكسجين كعامل:
أ- مؤكسد عند تفاعله مع الكلور.
ب- مختزل عند تفاعله مع الهيدروجين.
ج- مؤكسد عند تفاعله مع الفلور.
د- مختزل عند تفاعله مع المغنيسيوم.
- لديك الفلزات Cd , Cr , Ni , Mg وجميعها تكون على شكل أيونات ثنائية موجبة في مركباتها، فإذا علمت أنه:
- يمكن تحريك محلول MgSO4 بملعقة مصنوعة من الفلزات (Cd , Cr , Ni).
- يمكن تحريك محلول CdSO4 بملعقة من النيكل Ni ولا يمكن تحريكه بملعقة مصنوعة من الكروم Cr.
- يتحرر غاز الهيدروجين عند تفاعل الفلزات Cd , Cr , Ni , Mg مع حمض الهيدروكلوريك المخفف HCl .
فادرس المعلومات أعلاه، ثم أجب عن الفقرات (2، 3، 4)
2- الفلزان اللذان يكوّنان خلية جلفانية لها أعلى جهد معياري، هما:
أ- Ni/Cd
ب- Ni/Mg
ج- Cr/Mg
د- Cr/Cd
3- العنصر الذي يستطيع اختزال أيونات Cr2+ هو:
أ- Cd
ب- H2
ج- Mg
د- Cr
4- الترتيب الصحيح لأيونات الفلزات تبعاً لقوتها بصفتها عوامل مؤكسدة هي:
أ- Ni2+ < Cd2+ < Cr2+ < Mg2+
ب- Mg2+ < Cd2+ < Cr2+ < Ni2+
ج- Ni2+ < Cr2+ < Cd2+ < Mg2+
د- Mg2+ < Cr2+ < Cd2+ < Ni2+
5- عدد تأكسد جميع ذرات عناصر المجموعة السابعة (الهالوجينات) يساوي:
أ- (-1) في جميع مركباتها.
ب- (+1) في مركباتها الأيونية.
ج- (+1) في مركباتها التي تحتوي على الأكسجين.
د- (-1) في مركباتها الأيونية.
6- عدد مولات OH- اللازم إضافتها إلى طرفي المعادلة لموازنتها في وسط قاعدي يساوي:
Al + NO3- → AlO2- + NH3
أ- 3
ب- 4
ج- 5
د- 6
7- يتصاعد غاز الهيدروجين عند أحد أقطاب خلية جلفانية مكونة من قطب الهيدروجين المعياري وقطب الفلز (X). فإن العبارة الصحيحة المتعلقة بهذه الخلية، هي:
أ- يمكن حفظ حمض HCl في وعاء من فلز X
ب- ينحرف مؤشر الفولتميتر باتجاه قطب X
ج- قيمة جهد الخلية المعياري Eo سالبة.
د- X عامل مختزل أقوى من الهيدروجين.
- بناءً على المعلومات الواردة في الجدول المجاور، أجب عن الأسئلة (8، 9، 10) علماً بأن (جهد الاختزال المعياري للهيدروجين يساوي صفراً).
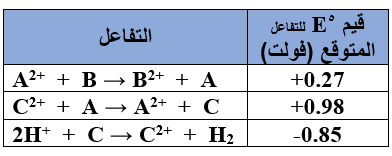
8- قيمة الجهد المعياري (Eo فولت) لخلية جلفانية قطباها (B/C) تساوي:
أ- +0.89
ب- +0.45
ج- +1.25
د- +0.125
9- العامل المختزل الأضعف هو:
أ- A
ب- B
ج- C
د- H2
10- إذا علمت أن قيمة جهد اختزال Y2+ = (-0.23 V) فإن الفلز Y يكون مهبطاً في خلية جلفانية قطباها:
أ- Y/A
ب- Y/B
ج- Y/C
د- Y/H2
دورة 2022
اختر الإجابة الصحيحة في كل فقرة مما يأتي، ثم ظلل بشكل غامق الدائرة التي تشير إلى رمز الإجابة في نموذج الإجابة (ورقة القارىء الضوئي) فهو النموذج المعتمد (فقط) لاحتساب علامتك، علماً بأن عدد الفقرات (10):
1- مقدار التغير في عدد تأكسد الكلور Cl يساوي (2) في:
أ- ClO- → ClO3-
ب- Cl2 → Cl2O
ج- HCl → Cl2
د- ClO3- → ClO4-
2- يبين الجدول المجاور جهود الاختزال المعيارية لعدد من الأيونات، فإن العنصر الأكثر ميلاً للتأكسد هو:

أ- Fe
ب- Ag
ج- Ca
د- H2
3- يسلك الهيدروجين عاملاً مؤكسداً في التفاعل:
أ- 2H2 + O2 → 2H2O
ب- H2 + 2Li → 2LiH
ج- N2 + 3H2 → 2NH3
د- H2 + Cl2 → 2HCl
- يبين الجدول المجاور تفاعلات تحدث في خلايا جلفانية في الظروف المعيارية، ادرسه ثم أجيب عن الفقرات (4، 5، 6)
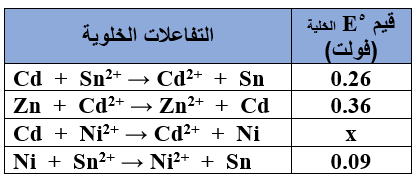
4- خلية جلفانية لها الجهد المعياري الأعلى قطباها:
أ- Cd/Zn
ب- Ni/Cd
ج- Sn/Zn
د- Ni/Sn
5- تترتب أيونات الفلزات وفقاً لقوتها كعوامل مؤكسدة:
أ- Zn2+ < Sn2+ < Ni2+ < Cd2+
ب- Cd2+ < Ni2+ < Zn2+ < Sn2+
ج- Ni2+ < Zn2+ < Sn2+ < Cd2+
د- Zn2+ < Cd2+ < Ni2+ < Sn2+
6- إذا كان جهد الاختزال المعياري لـ Sn2+ = (-0.14 V) فإن قيمة x (فولت) تساوي:
أ- 0.17
ب- 0.63
ج- 0.35
د- 0.47
- ادرس المعلومات الآتية للفلزات التي لها الرموز الافتراضية (M, Z, Y, X) وجميعها تكون على شكل أيونات ثنائية موجبة الشحنة في مركباتها، ثم أجب عن الفقرتين (7، 8)
- تستطيع أيونات الفلزات M, Y, Z أكسدة الفلز X .
- الفلز Z يختزل أيونات الفلز M من محاليله ولا يختزل أيونات الفلز Y من محاليله.
7- العبارة الصحيحة:
أ- لا يمكن حفظ محلول أحد أملاح X في وعاء مصنوع من الفلز Y
ب- العامل المختزل الأضعف X
ج- يمكن تحريك محلول الفلز Y بملعقة مصنوعة من الفلز Z
د- الخلية التي يكون لها جهد معياري أعلى قطباها X/Y
8- في الخلية الجلفانية قطباها M/Z :
أ- القطب Z مهبط
ب- تقل كتلة القطب M
ج- القطب M مصعد
د- يقل تركيز أيونات M
9- عدد جزيئات الماء H2O الناتج عن موازنة المعادلة:
HSO3- + IO3- SO42- + I2
أ- 2
ب- 1
ج- 6
د- 5
10- خلية جلفانية قطباها A/B إذا علمت أن:
- أيونات الفلز A تستطيع أكسدة الفلز B
- قيم جهود الاختزال المعيارية لقطبي الخلية (-0.18 V) و (-0.76 V) فإن قيمة:
أ- Eoreduction (B) = -0.18 V
ب- Eoreduction (A) = -0.76 V
ج- Eocell = 0.94 V
د- Eocell = 0.58 V
الدورة التكميلية 2022
اختر الإجابة الصحيحة في كل فقرة مما يأتي، ثم ظلل بشكل غامق الدائرة التي تشير إلى رمز الإجابة في نموذج الإجابة (ورقة القارىء الضوئي) فهو النموذج المعتمد (فقط) لاحتساب علامتك، علماً بأن عدد الفقرات (10):
1- نصف التفاعل الذي يزداد عدد تأكسد النتروجين (N) فيه بمقدار (4)، هو:
أ- N2H4 → NO
ب- NO2 → N2O4
ج- NO → N2
د- NO2- → NO3-
2- في المعادلة MnO4- + NO2 → MnO2 + NO3- ، فإن العبارة الصحيحة:
أ- يقل عدد التأكسد لذرة N بمقدار (1).
ب- يزداد عدد التأكسد لذرة Mn بمقدار (3).
ج- NO2 عاملاً مختزلاً.
د- MnO2 عاملاً مؤكسداً.
3- عدد الإلكترونات المفقودة أو المكتسبة اللازم لموازنة التفاعل الآتي في الوسط الحمضي، يساوي:
ICl → IO3- + I2 + Cl-
أ- 2
ب- 4
ج- 6
د- 8
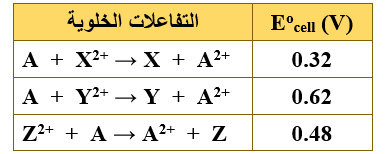 يبين الجدول المجاور عدداً من التفاعلات التي تتم في عدد من الخلايا الجلفانية أقطابها فلزات لها رموز افتراضية مع قيم (Eocell)، ادرسه، ثم أجب عن الفقرتين (4، 5)
يبين الجدول المجاور عدداً من التفاعلات التي تتم في عدد من الخلايا الجلفانية أقطابها فلزات لها رموز افتراضية مع قيم (Eocell)، ادرسه، ثم أجب عن الفقرتين (4، 5)
4- الترتيب الصحيح للرموز الافتراضية لعناصر فلزية وفقاً لقوتها كعوامل مختزلة:
أ- A < X < Z < Y
ب- Y < Z < X < A
ج- Z < Y < X < A
د- A < Z < Z < Y
5- إذا علمت أن الفلز الذي له الرمز الافتراضي M يستطيع اختزال أيونات الفلز Y ولا يستطيع اختزال أيونات الفلز Z فإن العبارة الصحيحة:
أ- يمكن تحريك محلول الفلز Y بملعقة مصنوعة من M
ب- يمكن حفظ محلول M في وعاء مصنوع من Z
ج- في الخلية Y/M تقل كتلة القطب M
د- Z عامل مختزل أضعف من M
- ادرس المعلومات الآتية، ثم أجب عن الفقرتين (6، 7)
- (C , D , W) فلزات لها رموزاً افتراضية.
- C → C2+ + 2e- (Eooxidation = 0.23 V)
- D → D2+ + 2e- (Eooxidation = -0.34 V)
- قيمة جهد الاختزال المعياري للهيدروجي تساوي صفراً.
- W هو القطب الموجب في الخلية الجلفانية قطباها (W/H2) قيمة (Eocell = 1.5 V).
6- الخلية الجلفانية التي لها أقل جهد معياري (Eocell):
أ- D/C
ب- D/H2
ج- C/H2
د- C/W
7- قيمة جهد الخلية المعياري (Eocell) للخلية الجلفانية قطباها W/D ، يساوي بوحدة (V):
أ- 1.84
ب- 1.16
ج- 1.24
د- 1.61
 يتضمن الجدول المجاور خلايا جلفانية في الظروف المعيارية، أقطابها فلزات لها رموز افتراضية (X,Y,Z,W) والتي تكون ثنائية الشحنة الموجبة في مركباتها، بالإضافة إلى قطب الهيدروجين المعياري. علماً أن (جهد الاختزال المعياري للهيدروجين يساوي صفراً) أجب عن الفقرات (10 , 9 , 8)
يتضمن الجدول المجاور خلايا جلفانية في الظروف المعيارية، أقطابها فلزات لها رموز افتراضية (X,Y,Z,W) والتي تكون ثنائية الشحنة الموجبة في مركباتها، بالإضافة إلى قطب الهيدروجين المعياري. علماً أن (جهد الاختزال المعياري للهيدروجين يساوي صفراً) أجب عن الفقرات (10 , 9 , 8)
8- في الخلية الجلفانية قطباها (Y/Z)، فإن العبارة الصحيحة:
أ- القطب Y يمثل القطب الموجب.
ب- يمكن تحريك محلول أيونات Z بملعقة من Y
ج- يستطيع العنصر Y اختزال أيونات Z من محاليله.
د- تتحرك الإلكترونات عبر الأسلاك من Z إلى Y
9- الأيون الذي يستطيع أكسدة عنصر الهيدروجين H2 :
أ- Z2+
ب- X2+
ج- Y2+
د- W2+
10- المعادلة التي تمثل التفاعل غير التلقائي:
أ- W2+ + Z → Z2+ + W
ب- Y + W2+ → W + Y2+
ج- Y2+ + X → Y + X2+
د- Z + 2H+ → Z2+ + H2
إعداد : شبكة منهاجي التعليمية
13 / 01 / 2023
النقاشات