تميه الأملاح
التميه: قدرة أيونات الملح على التفاعل مع الماء وإنتاج أيونات OH- أو H3O+ أو كليهما.
تستخدم تفاعلات التميه لتفسير سلوك الأملاح على النحو التالي:
- في محاليل الأملاح القاعدية (الناتجه من قاعدة قوية وحمض ضعيف):
يتميه الأيون السالب في الماء (لأنه يعطي حمضاً مرافقاً ضعيفاً) فيزيد من [OH-] في المحلول فتزداد قيمة pH فيصبح المحلول قاعدياً، بينما لا يتميه الأيون الأيون الموجب (لأنه يعطي قاعدة مرافقة قوية).
- في محاليل الأملاح الحمضية (الناتجه من حمض قوي وقاعدة ضعيفة):
يتميه الأيون الموجب في الماء (لأنه يعطي قاعدةً مرافقةً ضعيفةً) فيزيد من [H3O+] في المحلول فتقل قيمة pH فيصبح المحلول حمضياً، بينما لا يتميه الأيون الأيون السالب (لأنه يعطي حمضاً مرافقاً قوياً).
- في محاليل الأملاح المتعادلة (الناتجة من حمض قوي وقاعدة قوية):
لا يتميه الأيون الموجب في الماء (لأنه يعطي قاعدةً مرافقةً قويةً) فيبقى [H3O+] ثابتاً، ولا يتميه الأيون السالب (لأنه يعطي حمضاً مرافقاً قوياً) فيبقى [OH-] ثابتاً في المحلول، وتبقى قيمة pH ثابتة للماء.
ما الفرق بين عملية الذوبان وعملية التميه؟
عملية التميه تتضمن تفكك الملح إلى أيونات لها القدرة على التفاعل مع الماء، وتغيير تركيز أيونات H3O+ أو OH- في المحلول.
عملية الذوبان تتضمن تفكك الملح إلى أيونات ليس لها القدرة على التفاعل مع الماء، فيبقى تركيز أيونات H3O+ أو OH- في المحلول دون تغيير.
مثال (1):
اكتب معادلة تفسر التأثير القاعدي لمحلول ملح ايثانوات الصوديوم CH3COONa .
ملح ايثانوات الصوديوم مادة أيونية تتفكك في الماء وفق المعادلة:
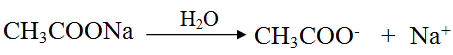
لا تتميه أيونات Na+ لأن مصدرها القاعدة القوية NaOH ، أما أيون الإيثانوات CH3COO- فيتميه لأنه يعطي حمض الإيثانويك الضعيف، حسب المعادلة:

فيؤدي ذلك إلى زيادة [OH-] ويصاحبه نقص في [H3O+] ، أي يرتفع الرقم الهيدروجيني (pH) نحو الجانب القاعدي (pH > 7).
مثال (2):
اكتب معادلة تفسر التأثير الحمضي لمحلول ملح كلوريد الأمونيوم NH4Cl .
ملح كلوريد الأمونيوم NH4Cl مادة أيونية تتفكك في الماء وفق المعادلة:
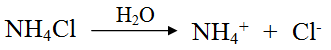
لا تتميه أيونات Cl- لأنها ناتجة من الحمض القوي (HCl)، أما الأيون NH4+ فيتميه لأنه ناتجٌ من القاعدة الضعيفة (NH3) حسب المعادلة التالية:

مما يؤدي إلى زيادة [H3O+] ونقصان الرقم الهيدروجيني ليصبح (pH < 7).
مثال (3):
فسر سبب كون محلول ملح كلوريد البوتاسيوم KCl متعادلاً.
ملح كلوريد البوتاسيوم KCl ملح متعادل يتفكك في الماء وفق المعادلة التالية:
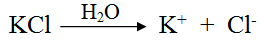
لا تتميه أيونات Cl- لأنها ناتجة من الحمض القوي (HCl)، كما لا يتميه الأيون K+ في الماء؛ لأن مصدرها القاعدة القوية KOH ، لذا فإن وجودهما في الماء لا يؤثر في قيمة الرقم الهيدروجيني.
سؤال 1 :
أي الأملاح الآتية يُعد ذوبانها في الماء تميهاً: KF , NaClO4 , CH3NH3Br ؟
سؤال 2 :
فسّر مستعيناً بمعادلات السلوك الحمضي أو القاعدي أو المتعادل لكل من الأملاح الآتية:
NaCN ، N2H5NO3 ، LiCl .
هل يمتلك ملح ما قدرة على التميه أكبر من غيره من الأملاح؟
نعم، فالملح الناتج من حمض أو قاعدة أضعف هو أكثر قدرةً على التميه.
سؤال 3 :
- أي محلولي الملحين أكثر قدرة على التميه: KCN أم NaF ؟
إذا علمت أن Ka لـ HCN = 6,2 × 10-10 ، Ka لـ HF = 7,2 × 10-4.
- أي محلولي الملحين أكثر قدرة على التميه: NH4Cl أم N2H5Cl ؟
إذا علمت أن Kb لـ NH3 = 1,8 × 10-5 ، Kb لـ N2H4 = 1,3 × 10-6.
إعداد : أ. أحمد الحسين
06 / 05 / 2022
النقاشات