الخصائص الدورية في الجدول الدوري
تتفاوت خصائص عناصر المجموعة الواحدة بالاتجاه من أعلى إلى أسفل، كما تتغير صفات العناصر في الدورة الواحدة بالاتجاه من يسار الجدول إلى يمينه، وتكون التغيرات في الخصائص متكررة في كل دورة، وتسمى تلك التغيرات المتكررة الدورية.
أهمية الدورية في الجدول الدوري
يستفاد منها في التنبؤ بسلوك العناصر وخصائصها، ومن الخصائص الدورية للعناصر الحجم الذري.
الحجم الذري
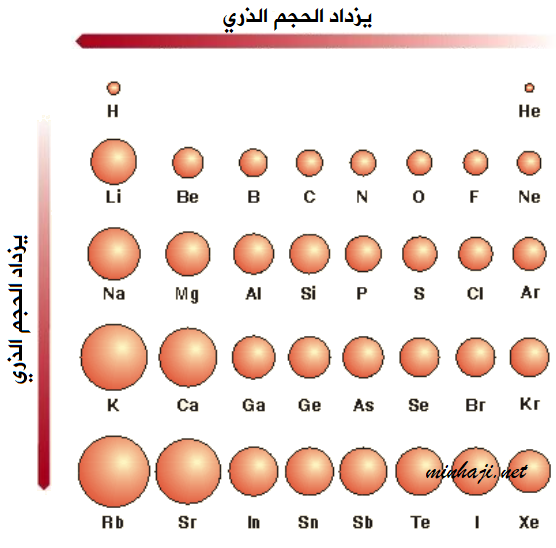
يتغير الحجم الذري للعناصر في الجدول التالي في الدورة والمجموعة على النحو الآتي:
- يزداد حجم الذرات بالانتقال من الأعلى إلى الأسفل في الجدول الدوري.
- يزداد حجم الذرات بالانتقال من اليمين إلى اليسار في الجدول الدوري.
أهمية دراسة الحجم الذري
يلعب الحجم الذري دوراً مهماً في تحديد صفات العناصر وسلوكها.
فمثلاً يزداد ميل الذرة لفقد الإلكترونات بزيادة حجمها؛ لأن قوة ارتباط الإلكترونات في مستوى الطاقة الخارجي بالنواة يصبح ضعيفاً بزيادة حجم الذرة.
سؤال:
بالرجوع إلى الجدول الدوري للعناصر، أي الذرات أصغر حجماً في الأزواج الآتية:
(F , Cl) ، (Na , Mg)؟
الإجابة:
الكلور أكبر حجماً من الفلور في الزوج الأول.
الصوديوم أكبر حجماً من المغنيسيوم في الزوج الثاني.
النشاط الكيميائي
تعلمت سابقاً أن الفلزات مرتبة في سلسلة تُسمى سلسلة النشاط الكيميائي.
سلسلة النشاط الكيميائي: ترتيب للفلزات وفق قدرتها على التفاعل.
ولكن ما علاقة نشاط الفلزات بموقعه في الجدول الدوري، وما علاقة نشاط الفلزات بحجمها؟
وما علاقة نشاط اللافلزات بموقعها في الجدول الدوري، ووما علاقة نشاط اللافلزات بحجمها؟
نشاط الفلزات
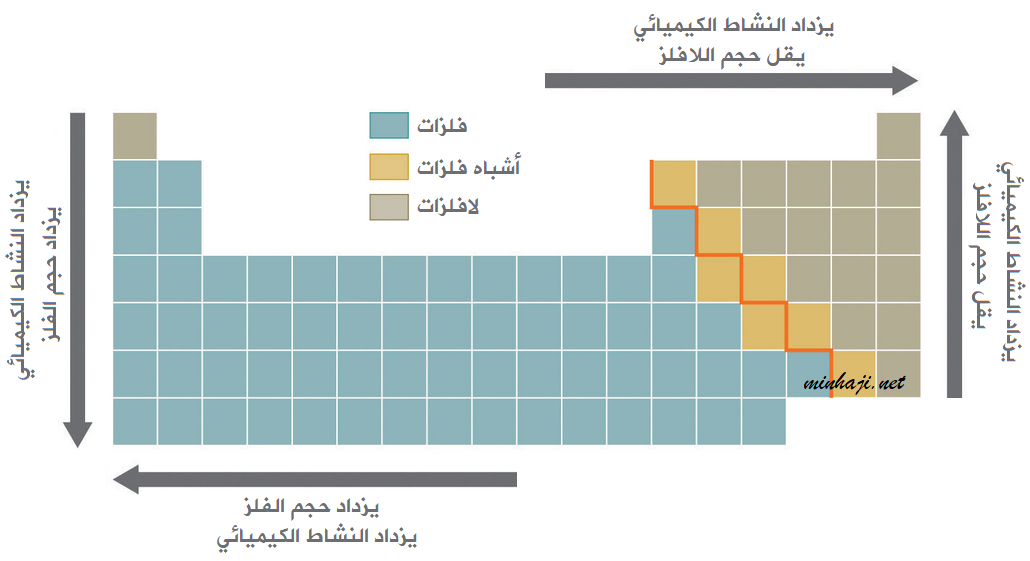
يزداد نشاط الفلزات بزيادة حجمها، فكلما زاد حجمها زادت قدرتها على فقد الإلكترونات، وعليه فإن السلوك الفلزي يزداد في الجدول الدوري بالاتجاه من اليمين إلى اليسار، ومن الأعلى إلى الأسفل.
نشاط اللافلزات
يزداد نشاط اللافلزات بنقصان حجمها، فكلما قل حجمها زادت قدرتها على كسب الإلكترونات، وعليه فإن السلوك اللافلزي يزداد في الجدول الدوري بالاتجاه من اليسار إلى اليمين، ومن الأسفل إلى الأعلى.
سؤال:
بالرجوع إلى الجدول الدوري التالي، أجب عن الأسئلة الآتية:
- أي العنصرين أكبر حجماً Cl أم F ؟
- أي العنصرين أنشط كيميائياً Cl أم F ؟
- اكتب معادلة كيميائية موزونة تمثل تفاعل المغنيسيوم Mg مع الكلور Cl.
الإجابة:
- الكلور أكبر حجماً؛ لأنه يقع تحت الفلور في الجدول الدوري.
- الفلور أنشط كيميائياً؛ لأنه أصغر حجماً، وفي اللافلزات يزداد النشاط بنقصان الحجم الذري.
- تفاعل المغنيسيوم مع الكلور:
Mg + Cl2 → MgCl2
إعداد : شبكة منهاجي التعليمية
03 / 09 / 2022
النقاشات