خصائص عناصر مجموعات الجدول الدوري
المجموعة الأولى: (1A)
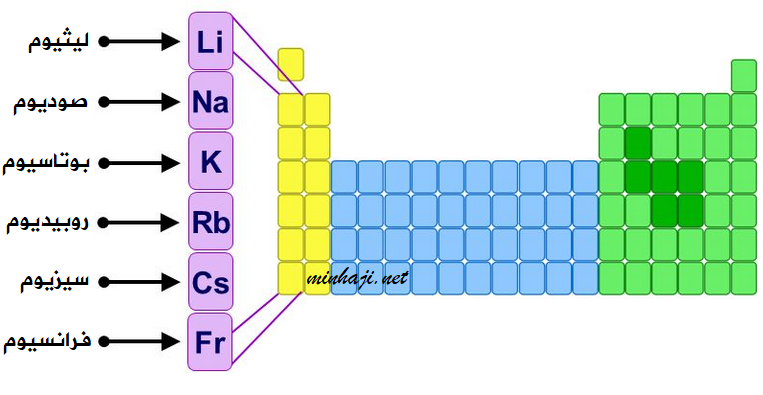
تشمل عناصر المجموعة الأولى عناصر أهمها: الليثيوم، والصوديوم، والبوتاسيوم،، والربيديوم.
تسمى الفلزات القلوية، باستثناء الهيدروجين.
الخصائص الفيزيائية لعناصر المجموعة الأولى
- لامعة.
- جميعها لينة يسهل قطعها بالسكين.
- ذات درجتي غليان وانصهار منخفضتان مقارنة بالفلزات الأخرى.
الخصائص الكيميائية لعناصر المجموعة الأولى
- تحتوى عناصر المجموعة الأولى على إلكترون واحد في مستوى الطاقة الخارجي لها.
- تميل للاستقرار عندما تفقد إلكتروناً وتصبح أيوناً أحادياً موجباً (1+).
التفاعل مع الهواء
تتفاعل بشدة مع الهواء؛ لذا تحفظ بمعزل عنه، فمثلاً يحفظ الصوديوم تحت الكاز،، ويحفظ البوتاسيوم تحت البرافين.
التفاعل مع الماء
تتفاعل بشدة مع الماء وتكون هيدروكسيدات الفلزات مثل هيدروكسيد الصوديوم NaOH ، ويتصاعد من تفاعلها مع الماء غاز الهيدروجين.
Na(s) + H2O(l) → NaOH(aq) + H2(g)
K(s) + H2O(l) → KOH(aq) + H2(g)
تتفاوت عناصر المجموعة في شدة تفاعلها مع الماء، فهو يزداد من أعلى إلى الأسفل تبعاً لزيادة نشاطها الكيميائي:
- يتفاعل الليثيوم مع الماء ببطء.
- يتفاعل الصوديوم مع الماء بشدة، وتؤدي الحرارة الناتجة إلى احتراق غاز الهيدروجين الناتج.
- تفاعل البوتاسيوم مع الماء شديد، إذ يؤدي إلى إنتاج كمية كبيرة من الطاقة تسبب اشتعالاً شديداص للهيدروجين.
- يؤدي تفاعل السيزيوم مع الماء إلى حدوث انفجار بسبب شدة التفاعل.
المجموعة الثانية: (2A)
تشمل عناصر المجموعة الثانية عناصر أهمها: البريليوم، والمغنيسيوم، والكالسيوم، والسترونشيوم، والباريوم.
تسمى الفلزات القلوية الأرضية؛ لأنها توجد في القشرة الأرضية على شكل صخور السيليكات والكربونات والكبريتات، وهي قليلة الذوبان في الماء.
أكثر الفلزات انتشاراً في القشرة الأرضية وأكثرها أهمية الكالسيوم والمغنيسيوم.
الخصائص الفيزيائية لعناصر المجموعة الثانية
- جميعها فلزات.
- تعتبر أكثر صلابة وكثافة من عناصر المجموعة الأولى.
الخصائص الكيميائية لعناصر المجموعة الثانية
- تحتوى عناصر المجموعة الثانية على إلكترونين في مستوى الطاقة الخارجي لها.
- تميل للاستقرار عندما تفقد إلكترونين وتصبح أيوناً ثنائياً موجباً (2+).
- القلويات الأرضية أقل نشاطاً من الفلزات القلوية.
- البريليوم أقل فلزات المجموعة نشاطاً، والباريوم أكثرها نشاطاً.
إعداد : شبكة منهاجي التعليمية
03 / 09 / 2022
النقاشات